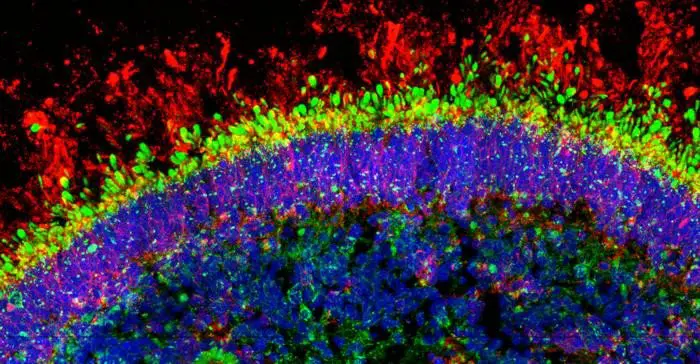
Врождённый амавроз Лебера (ВАЛ) относится к редким наследственным патологиям сетчатки глаза, проявляющимся уже в младенчестве выраженным снижением остроты зрения. На сегодняшний день ВАЛ диагностируется примерно у 2–3 из 100 000 новорождённых, оказывая глубокое влияние на качество жизни детей и их семей. В основе этого заболевания лежат генетические мутации, влияющие на белки, без которых работа клеток сетчатки невозможна.
Генетическое разнообразие при ВАЛ: вызовы и перспективы
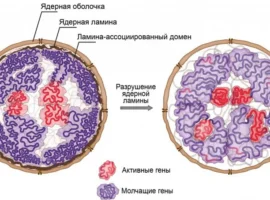
Причиной ВАЛ могут быть нарушения структуры более чем двадцати различных генов, причём только в одном из них зачастую выявляют сотни уникальных изменённых участков – генетических вариантов. Эти варианты делятся на нейтральные и патологические, причём первые никак не влияют на функционирование органов, а вторые зачастую приводят к стремительному прогрессированию потери зрения. Между этими категориями находятся так называемые варианты неопределённой значимости (VUS), точное влияние которых пока не известно.
Пионерские разработки команды Робин Джеймисон
Группа исследователей под руководством Робин Джеймисон, действующая на базе Института детских медицинских исследований Сиднейского университета, вывела диагностику на качественно новый уровень. Специалисты предложили уникальную лабораторную платформу, целью которой стала оценка VUS в гене RPGRIP1 – одном из ключевых для развития ВАЛ.
В качестве исследовательской базы были использованы органоиды сетчатки, созданные из стволовых клеток пациентов: один из них обладал уже подтверждёнными патогенными мутациями в RPGRIP1, а второй имел неизвестные ранее VUS в том же гене. Развитые лабораторные модели воспроизводят строение и функции человеческой сетчатки, позволяя наблюдать клеточные реакции на определённые генетические изменения в динамике.
Выявление патогенных изменений через органоиды
В органоидах обоих пациентов учёные обнаружили схожие аномальные признаки: заметно уменьшенное число фоторецепторов – клеток, отвечающих за световосприятие, а также изменение активности ряда критически важных генов. Это стало основанием для более глубокого анализа природы VUS.
Чтобы подтвердить роль подозрительных вариантов в развитии заболевания, исследователи внесли VUS RPGRIP1 в здоровые органоиды сетчатки. Результат оказался показательным – органоиды с модифицированным геном ответили аналогичными патологическими изменениями, отмеченными и у больных пациентов. Более того, возвращение в такие органоиды здорового варианта RPGRIP1 обратило негативные процессы, восстановив общее состояние клеточной структуры. Такой подход открывает двери к доказательному определению патогенности вариантов и, в перспективе, персонализированной терапии.
Применение инноваций – шаг навстречу эффективному лечению
Созданная платформенная модель стала первым инструментом, позволяющим функционально тестировать варианты RPGRIP1, ранее неизвестные науке. Это не только помогает быстрее выявлять новые случаи и классифицировать VUS как доброкачественные либо патогенные, но и серьёзно расширяет возможности индивидуальной диагностики.
Полученные в ходе работы знания закладывают фундамент для разработки целевых терапевтических подходов, а также для формирования персонализированных рекомендаций и генетического консультирования семей из группы риска. Благодаря усилиям Робин Джеймисон и её коллег из Института детских медицинских исследований Сиднейского университета, перспективы пациентов с ВАЛ становятся всё более благоприятными. Успехи этого научного коллектива внушают уверенность в скором появлении надёжных методов профилактики и лечения наследственных патологий сетчатки.
Оптимистичный взгляд в будущее офтальмологии
В своём инновационном проекте команда Сиднейского университета продемонстрировала, что интеграция современных клеточных технологий и точной генетической диагностики усиливает возможности медицины и вселяет надежду для пациентов с генетически обусловленными нарушениями зрения. Надежда на успешное восстановление и предотвращение слепоты становится всё более реальной благодаря новым научным открытиям, а команды учёных продолжают раздвигать горизонты возможностей, чтобы подарить миллионам людей шанс на качественную жизнь и полноценное зрение.
Источник: scientificrussia.ru